がん医療を拓く⑨ 諸刃の剣 細胞老化
細胞老化とは、正常な体細胞が分裂・増殖を止めてしまう現象を指します。約50年前に発見されました。
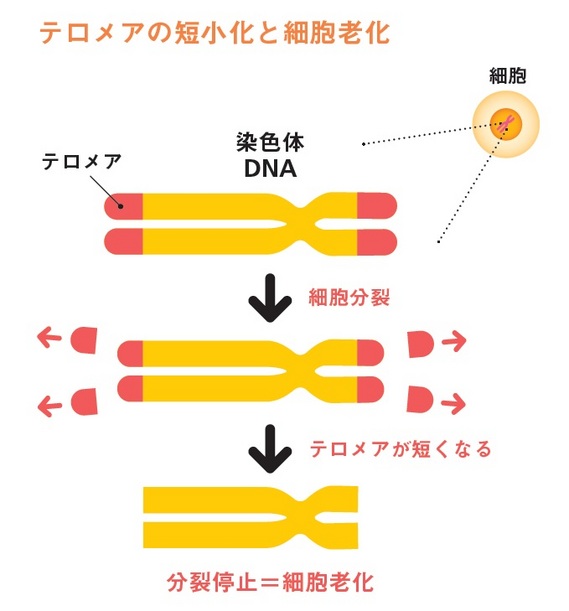
通常、正常な体細胞の染色体は、テロメアと呼ばれる一定の末端構造を持っています。テロメアは正常なDNA複製を助ける働きを持っていて細胞分裂の度に短くなっていき、ついには細胞分裂を停止させます。これが一つ目のパターンですが、テロメアが短くならなくても細胞老化は起きることがあります。
分裂を止めた細胞は、以後増えることはなく、かといって死ぬこともないまま、ただただ生き続けることになります。
細胞レベルでは発がん抑制
 あらかじめお断りしておくと、「細胞老化」は、体の機能や性状の衰えを意味する「老化」とは異なるものです。両者の間に相関がある可能性も指摘されていますが、未だ不明な点も多く残っています。
あらかじめお断りしておくと、「細胞老化」は、体の機能や性状の衰えを意味する「老化」とは異なるものです。両者の間に相関がある可能性も指摘されていますが、未だ不明な点も多く残っています。
確かに年齢を重ねれば細胞分裂も回数を重ねることになりテロメアは短くなりますが、分裂の頻度は臓器・器官や部位などによっても違い、また前述したようにテロメアが短くならなくても細胞老化は起きるので、個体の老化と細胞の老化は完全に同じというわけではありません。ただし今でも、名前が紛らわしいことから、両者を混同する研究者が多いのも事実です。
ストレスで起きる
話を戻します。がんは、細胞が無限に増殖をしてしまうものです。増殖を止めるという細胞老化の性質から、早い段階から、がん抑制機構ではないかと考えられてきました。しかしメカニズムの解明が進んでいませんでした。
「それがこの30年ほどで、遺伝子レベルで制御されていることが次第に明らかになってきたのです」と話すのは、がん研究会がん研究所がん生物部の原英二部長。
「私たちは、正常な体細胞が限界まで分裂した場合、p16という遺伝子の発現が上昇して細胞老化を起こすことを発見しました。このような細胞老化遺伝子は他にもいくつか確認されています」
また原部長らは、マウス生体内に老化細胞が蓄積していく様子をリアルタイムに可視化することに成功しました。さらにp16遺伝子の働きを失わせたマウスでは発がんが促進されることも確認しました。細胞老化が、生体内でがん抑制機構として働くことを示したのです。
p16は元々がん抑制遺伝子として発見されたものです。多くのヒトのがんで働きが失われている一方、正常な細胞でも普段はほとんど働いていないので、どうやって発がんを抑制しているのか長らく謎でしたが、その方法が突き止められたことになります。
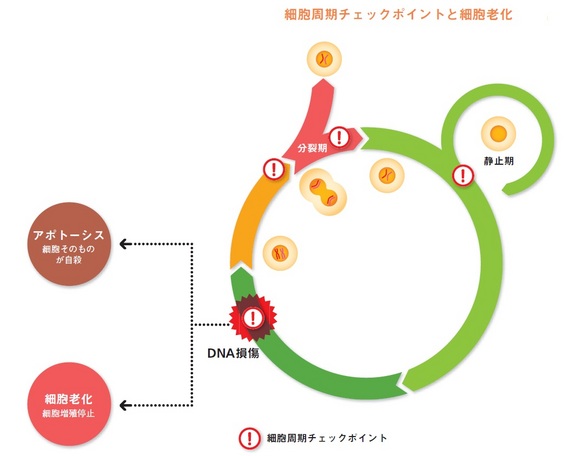
細胞分裂の周期には途中、複数のチェックポイントがあり、DNAに異常がないか確認が行われます。正常ならばそのまま増殖へと進みますし、損傷や異常があれば修復が試みられます。損傷や異常が大き過ぎる場合は、細胞そのものが自殺します(アポトーシス)。問題は、修復できないけれどもアポトーシスにも及ばない「中途半端なダメージ」の場合です。そのまま増殖させてしまっては、がん化しかねません。
「そこで生物の獲得した自衛手段が細胞老化なのです。がん遺伝子に変異が起きたり、放射線や紫外線などでDNAが傷ついたり、様々な発がんストレスにさらされた場合に、p16等の発現は著しく上昇することが分かりました」
何らかの発がんストレスにさらされDNAに異常が出た場合、アポトーシスか細胞老化によって、がん化を回避するというわけです。(図参照)
原部長は細胞老化の分かりやすい例として「ほくろ」を挙げます。確かにほくろは、皮膚が新陳代謝を繰り返しても消えずに、いつまでも同じような大きさで存在し続けますね(急にほくろが大きくなった場合は、メラノーマという皮膚がんも疑われます。早めの受診を!)。
このように発がん抑制機構であるはずの細胞老化ですがが、近年、全く逆に発がんを促すことも分かってきました。

