がん医療を拓く⑨ 諸刃の剣 細胞老化
蓄積が進むと万病の元に
発がんを促進する働きも持っているとは、どういうことでしょうか。原部長は二つの経路を挙げます。
一つ目は、細胞老化を起こした細胞がDNAに異常を抱えたまま生き続けているということです。再び増殖を始めれば、がん化しかねません。
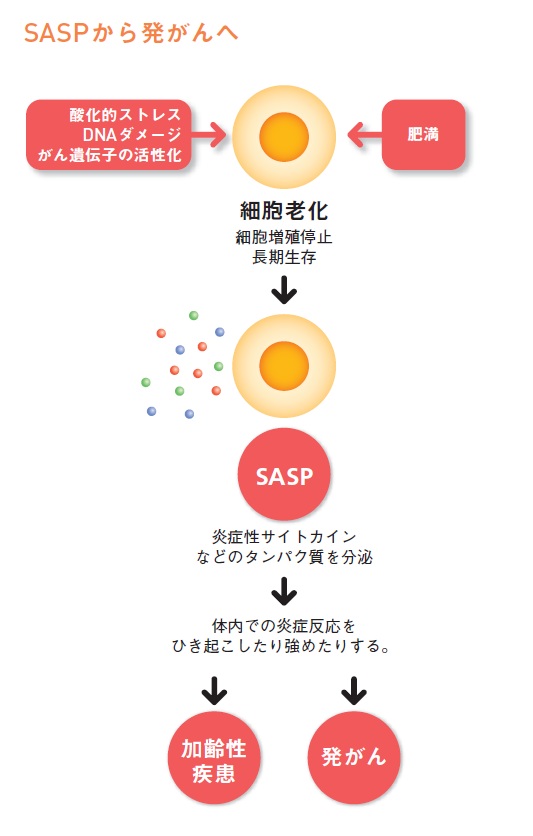
二つ目は、細胞老化を起こした細胞が、じっとおとなしくしていてくれるわけではなく、次第に炎症性サイトカインなど様々なタンパク質を分泌するようになることです。この現象は最近明らかになってきたもので「SASP」と呼ばれます。(図参照)
炎症性サイトカインは体内の炎症反応をひき起こしたり強めたりします。慢性炎症が発がんや転移を促進することは、長らく経験的に認識されてきており、近年では分子レベルで説明されるようになってきています。
「ですから細胞老化は、短期的にはがん抑制機構として働くものの、長期的に蓄積していくほどに、がん促進に働いてしまうんです」と原部長。まさに諸刃の剣だったというわけです。
「また最近の研究から、SASPは肥満によっても誘導されることが分かってきています。肥満に伴って発がん頻度の上昇する原因の一つが、細胞老化にあると考えられるんです」
がんだけではありません。今日では、様々な病気の裏側にも慢性炎症は潜んでいることが明らかになってきています。
「SASPによってばら撒かれる炎症性サイトカインは、リウマチや心血管疾患、骨粗鬆症をひき起こしたり悪化させたりする原因としても研究が進んでいます」
要するに、多くの加齢性疾患に、細胞老化の負の産物であるSASPが関与している可能性は高いのです。
想定外の長寿で
生体防御機構として発達したはずの細胞老化が、どうしてそんな不都合を抱えているのでしょう。原部長の解説は示唆に富んでいます。
「増殖停止は酵母菌にも見られるくらいですから、細胞老化はおそらく生物進化のかなり早い段階で、生体防御機構として組み込まれてきたのでしょう。ただしヒトという生物が出現して、これほど長寿になるのは想定外だったはずです。今から100年ほど前、日本人の平均寿命はたった約40年、米国でも50年でした。つい最近までSASPの影響が出てくる前に寿命を迎えていたのです」
ちなみに、マウスでも同じことが確認されています。野生ならば3~4カ月で死んでいくのに対して、清潔で栄養十分の管理環境にいると2年ほども生きますが、生後6カ月を過ぎたところでp16遺伝子の発現が上がり、最後はがんで死んでいくのだとか。
だったら細胞老化を防げばよいのかというと、完全に抑制した場合には、かえって様々な病態をひき起こすことも分かっているそうです。やはり生体防御機構には違いないわけですね。
そこで原部長らは現在、細胞老化そのものでなくSASPの誘導を抑制することで、加齢に伴うがんの治療や予防、診断方法の開発につなげたいと、メカニズムの解明を続けています。SASPを回避する術が確立すれば、他の加齢性疾患の治療や予防も一気に進むかもしれません。健康長寿を望むすべての人々の期待がかかった研究と言えそうです。
