国内未承認の抗がん剤を迅速に保険適用へ
■ 厚労省課長の説明②
[保険局医療課・鈴木康裕課長]
この(資料の)中身を見ていただきますと、文章編で3ページまで書いてございますけれども、恐らく文章編よりはポンチ絵の方が分かりやすいと思いますので、4ページ以降をちょっとご覧いただきたいと思います。
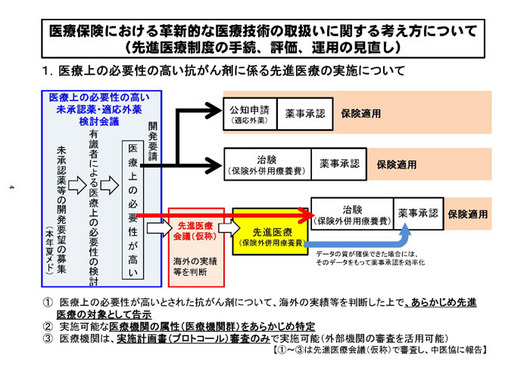 3点、ございます。まず1点目でございますけれども、特に抗がん剤にかかるものとして......。これは中医協でもご議論が出ていましたけれども、いわゆる(厚労省医薬食品局の)未承認薬検討会というものがございます。
3点、ございます。まず1点目でございますけれども、特に抗がん剤にかかるものとして......。これは中医協でもご議論が出ていましたけれども、いわゆる(厚労省医薬食品局の)未承認薬検討会というものがございます。
ここで、開発について「医療上の必要性が高い」とされたものについて基本的には開発要請を各企業にかけていただいて、これを既にご議論いただいた公知申請なり、もしくは新たに治験をしていただいて最終的には薬事承認をしていただくことが本筋だと思います。
ただし、それ以外のもの......、例えば日本において該当する企業がないとか、手が挙がらない等々の理由によるもの等については......。
あとでちょっと申し述べますが、「先進医療会議」(仮称)というものを経由いたしまして、先進医療を実施していただいて、ここで一定の質のデータ......、のものが得られた場合には、薬事承認にそれを活用していただきたいということを考えております。
(図の)下に①から③まで書いてありますけれども、これをもう少しポンチ絵的に分かりやすくしたのが資料の6ページ目でございます。
左側が現在の姿、右側がこれから......、ご承認いただければこういうことにしたい、ということでございます。
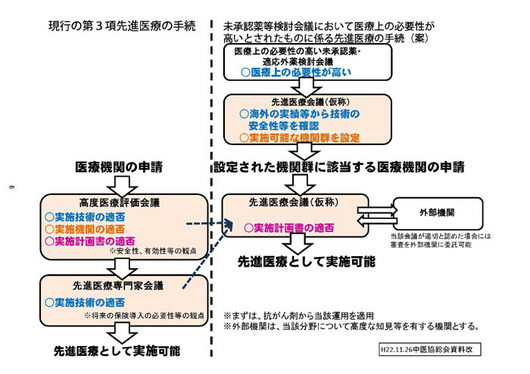 何かと申し上げますと、現在、医療機関からの申請について3つの審査をしております。1つは、技術としてどうかということが1つ。
何かと申し上げますと、現在、医療機関からの申請について3つの審査をしております。1つは、技術としてどうかということが1つ。
もう1つは、実施される機関が適か否かということ。さらには、実際に研究をしていただく、「プロトコール」と言いますけれども、実施計画がどうかという、この3つの観点について議論をしていただいているわけですけれども......。
先ほど申し上げました未承認薬検討会で、既に「医療上の必要性が高い」とされたものについては、技術についてはそこで認めましょうと。それからさらに、実際に手が挙がる前に、一定の実施可能な機関群というのを特定いたしましょうと。
ということになりますと、あと実際に審査するのは実施計画のみということになります。
ちょっと(ページ)戻って恐縮ですけれども、じゃ、機関としてどういう所を考えているかということにつきましては、1ページにちょっとお戻りいただいて......。
 一番下の丸、下線部以下でございますけれども、「医療機関の施設属性」と書いてありますが、臨床研究中核病院......、ICH-GCPと書いてありますが、国際的な臨床試験の基準でございますけれども、そういうものを充たす病院。
一番下の丸、下線部以下でございますけれども、「医療機関の施設属性」と書いてありますが、臨床研究中核病院......、ICH-GCPと書いてありますが、国際的な臨床試験の基準でございますけれども、そういうものを充たす病院。
あとは、都道府県のがん診療連携拠点病院、それから特定機能病院等というのを現在のところイメージをしております。これがまず1点目でございます。
【目次】
P1 → 厚労省課長の説明①
P2 → 厚労省課長の説明②
P3 → 厚労省課長の説明③
P4 → 「非常に進歩したと評価したい」 ─ 嘉山委員
P5 → 「審査の効率化、重点化はいい」 ─ 小林委員
P6 → 「現在の評価基準を総会で議論して」 ─ 安達委員
P7 → 「公正性を担保するような制度にして」 ─ 花井委員
P8 → 「お金を払えば受けられるようになるのか」 ─ 西村委員
