再生医療の運営費、年3000万円超
 ヒアリングで澤委員は、「未来医療センター」を運営する人員体制や設備などを紹介した上で、「今日申し上げたいのはここからだ」と強調し、次のように述べた。
ヒアリングで澤委員は、「未来医療センター」を運営する人員体制や設備などを紹介した上で、「今日申し上げたいのはここからだ」と強調し、次のように述べた。
「300平方メートルのCPCの運営経費は年間3000万円。昨年は10例しか行っていないので、1例につき300万円ぐらい掛かっている。今後、これをどうしていくか、(未来医療)センター長として非常に悩ましいし、力の入れ所だろうと思っている」
その上で、「GMP基準のハードルが高ければ高い程、全国60か所のCPCが運営していけるのかを案じる。今は公的な資金がCPC設置に回っているが、このまま放っておくと、資金が切れるころには細胞培養室が倉庫になってしまうことになりかねない」と現状を訴えた。
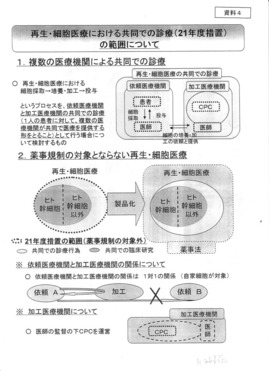 医薬品や血液製剤などの製造は、薬事法に基づく品質管理の基準「GMP(Good Manufacturing Practice)」で規制されている。
医薬品や血液製剤などの製造は、薬事法に基づく品質管理の基準「GMP(Good Manufacturing Practice)」で規制されている。
しかし、細胞の治療や再生医療に使う細胞の製造(培養・加工)に対する規制は不明確になっている。
例えば、A病院が血小板製剤を院内で製造して同院の患者に投与することは、薬事法(GMP)と医療法の基準をクリアすれば許されるが、この血小板製剤を別のB病院の患者に投与することは認められていない。
しかし、A病院での製造が一定の基準を満たしていればB病院の患者に投与することを認めるべきではないか、さらに医療機関同士だけでなく企業の参加も認めるべきではないかなどが問題となっている。

>臓器移植や人工臓器に代わる切り札として注目される「再生医療」
iPS細胞やES細胞などは、いくつかのトライアルのうち一部が組織レベルで分化が認められたレベルに過ぎず、臓器への分化や発がん性の問題などまだまだ克服すべき課題が多いようですね。(マウスだかラットの背中に耳介を作った写真を見た覚えはありますが、きちんと機能する臓器はまだまだ先ですね。)
私はむしろ、ヒトに対する抗原性タンパクをノックアウトしたクローン動物(ミニブタなど)を更に改良した「異種移植」が臨床的には実現可能性としては早いのではないかと個人的には予想しています。あまり抵抗感がなく、急性拒絶反応時にもリカバーしやすい臓器や組織から、まずは始まるのではないかとは思いますが。